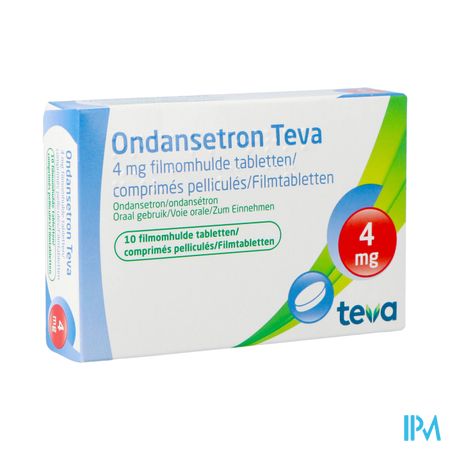
Ondansetron Teva Comp Pell 10 X 4mg
Op voorraad
Onze Leveringsmethodes:
Afhaling in de apotheek
Levering aan huis
Dit is een geneesmiddel, geen langdurig gebruik zonder medisch advies, bewaren buiten bereik van kinderen, lees aandachtig de bijsluiter. Vraag raad aan uw arts of apotheker. In geval van bijverschijnselen, neem contact met uw huisarts.
Geneesmiddelen zijn geen gewone producten. Ze kunnen nooit teruggenomen of geruild worden. De wet verbiedt apothekers om ongebruikte geneesmiddelen terug te nemen. In het belang van uw veiligheid worden alle geneesmiddelen die u terugbrengt naar de apotheek gesorteerd bij de vervallen geneesmiddelen.
Lees meer over Indicatie , Samenstelling , Bijwerkingen , Contra indicatie , Gebruik , Gegevens en Bijsluiter .
Preventie en behandeling van misselijkheid en braken:
- veroorzaakt door cytotoxische chemotherapie;
- veroorzaakt door radiotherapie met een toegediende dosis gelijk aan of hoger dan 1,5 Gy per
behandeling op een oppervlakte waarvan minstens een deel gelegen is tussen de wervels D11 en
L3;
- veroorzaakt door radiotherapie toegediend in een enkele dosis gelijk aan of hoger dan 8 Gy.
Preventie en behandeling van misselijkheid en braken na een operatieve ingreep gedurende de 24 uur die
volgen op de inductie van de algemene anesthesie bij risicopatiënten met een verlaagde emetogene
drempel.
Elke filmomhulde tablet bevat 4 mg ondansetron, als ondansetronhydrochloridedihydraat (5 mg).
Hulpstof met bekend effect: Elke filmomhulde tablet bevat 88,8 mg lactosemonohydraat.
Lactosemonohydraat, natriumzetmeelglycolaat (type A), microkristallijne cellulose, gepregelatineerd
zetmeel, magnesiumstearaat, hydroxypropylmethylcellulose, titaandioxide (E171), macrogol 400, macrogol
6000, ijzeroxide geel (E172)
- Mogelijke bijwerkingen
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben. Niet iedereen krijgt daarmee te maken.
Verwittig onmiddellijk uw arts als u één van de volgende symptomen voelt na het innemen van Ondansetron Teva :
zelden, allergische reacties (die zich kunnen voordoen als huiduitslag, zwelling van de lippen, het gelaat en de oogleden, hartkloppingen, een drukkend gevoel op de borstkas of een piepende ademhaling), zeer zelden, anafylactische reacties (ernstige vorm van onmiddellijk allergie), myocardischemie
Tekenen zijn onder meer: - plotselinge pijn op de borst of - drukkend gevoel op de borst.
Neem uw geneesmiddel niet meer in totdat uw arts u advies heeft gegeven. Het is mogelijk dat uw arts beslist om uw behandeling stop te zetten.
Andere bijwerkingen die kunnen voorkomen :
Zeer vaak (kunnen voorkomen bij meer dan 1 op de 10 mensen) hoofdpijn.
Vaak (kunnen voorkomen bij maximaal 1 op de 10 mensen) warmtegevoel en warmteopwellingen (fel rood gezicht), constipatie.
Soms (kunnen voorkomen bij maximaal 1 op de 100 mensen) onwillekeurige bewegingen of beven, maar zonder blijvende gevolgen, stuipen (bij epilepsiepatiënten), pijn ter hoogte van de borstkas, een onregelmatige of abnormaal trage hartslag of te lage bloeddruk, de hik, gestoorde resultaten van een bloedonderzoek om de werking van de lever te controleren.
Zelden (kunnen voorkomen bij maximaal 1 op de 1.000 mensen) hartritmestoornissen (die soms een plotseling bewustzijnsverlies veroorzaken).
Zeer zelden (kunnen voorkomen bij maximaal 1 op de 10.000 mensen) veralgemeende huiduitslag met blaren en afschilfering van de huid over een groot gedeelte van het lichaamsoppervlak (toxische epidermale necrolyse).
Wanneer mag u dit geneesmiddel niet gebruiken?
U neemt apomorfine in om de ziekte van parkinson te behandelen.
U bent allergisch voor een van de stoffen in dit geneesmiddel. Deze stoffen kunt u vinden in rubriek 6 van deze bijsluiter.
A) Misselijkheid en braken veroorzaakt door chemotherapie en radiotherapie
Het emetogeen vermogen van een cytotoxische chemotherapie en van een radiotherapie is afhankelijkvan de dosis, van de gebruikte combinatie van cytostatica en van de individuele gevoeligheid van elkepatiënt.
Ondansetron kan zowel rectaal, oraal (tabletten of siroop), intraveneus of intramusculair toegediendworden. Voor jonge kinderen zijn aangepaste farmaceutische vormen beschikbaar.
- Volwassenen.
Zeer emetogene chemotherapie
Bij patiënten die behandeld worden met sterk emetogene chemotherapie, zoals bijvoorbeeld hogedoses cisplatine, kan ondansetron zowel rectaal, intraveneus als intramusculair worden toegediend.24 uren na de chemotherapie zal de behandeling via orale weg worden verder gezet a rato van 8 mgper os (2 tabletten) om de 12 uur. De duur van de behandeling bedraagt doorgaans 3 tot 5 dagen nahet einde van de chemotherapie.
Alle vermelde farmaceutische vormen zijn in België niet te koop.
Minder emetogene chemotherapie
Vóór de aanvang van de chemotherapie: 8 mg per os (2 tabletten), 1 à 2 uur vóór de aanvang van dechemotherapie. Deze eerste toediening moet gevolgd worden door een behandeling met 8 mg per os(2 tabletten) om de 12 uur. De duur van deze behandeling bedraagt doorgaans 3 - 5 dagen na heteinde van de chemotherapie.
Radiotherapie
Vóór de radiotherapie: 8 mg per os (2 tabletten), 1 à 2 uur vóór de aanvang van de radiotherapie.Deze eerste toediening kan indien nodig vervolgd worden door 8 mg per os (2 tabletten) om de 12 uur.De duur is afhankelijk van de duur van de radiotherapeutische behandeling.
- Pediatrische patiënten.
Bij kinderen ouder dan 2 jaar bleek Ondansetron Teva werkzaam en goed verdragen. De posologiebedraagt 5 mg/m² gedurende 15 minuten in intraveneus infuus, onmiddellijk vóór dechemotherapie.
Vervolgens wordt 4 mg per os (1 tablet) om de 12 uur toegediend. De duur van de behandelingbedraagt doorgaans 3 tot 5 dagen na het einde van de chemotherapie.
- Bejaarde patiënten.
De werkzaamheid en de tolerantie bij patiënten ouder dan 65 jaar is gelijkaardig aan die bij jongepatiënten. De toediening aan bejaarde patiënten vereist dus geen aanpassing van de dosis of vande toedieningswijze
B) Postoperatieve misselijkheid en braken.
- Volwassenen.
a.) Preventie: toedieningsweg: intraveneus, intramusculair of oraal. Voor orale toediening:8 mg (2 tabletten), één uur voor de inductie van de anesthesie, gevolgd door 16mg (4tabletten) om de 8 uren.
b.) Behandeling: intraveneuze of intramusculaire toediening wordt aanbevolen.
- Pediatrische patiënten. Toediening als langzame intraveneuze injectie wordt aanbevolen.
- Bejaarden. De beschikbare gegevens zijn onvoldoende om een posologie aan te bevelen bijdeze patiënten.
Alle vermelde farmaceutische vormen zijn in België niet te koop.
C) Nierinsufficiëntie.
Toediening van Ondansetron Teva aan patiënten met nierinsufficiëntie vereist geenaanpassing van posologie of toedieningsweg.
D) Leverinsufficiëntie.
De klaring van ondansetron is significant verminderd en de plasmahalveringstijd significantverlengd bij patiënten met matig ernstig of ernstig verminderde leverfunctie. De totale dagdosiszal 8 mg niet overschrijden bij deze patiënten.
E) Patiënten met trage sparteïne/debrisoquine metabolisatie.
De halveringstijd van ondansetron is bij patiënten die tot deze groep behoren, niet verschillend.Bij herhaalde toediening is er geen concentratiestijging in vergelijking met de zogenaamdnormale populatie. Een aanpassing van de posologie is dus niet vereist.
| CNK | 2547057 |
|---|---|
| Organisaties | Arega, Teva Belgium |
| Merken | Teva |
| Breedte | 73 mm |
| Lengte | 108 mm |
| Diepte | 25 mm |
| Hoeveelheid verpakking | 10 |
| Actieve ingrediënten | ondansetron hydrochloride |
| Behoud | Kamertemperatuur (15°C - 25°C) |